- 検証サービス
- 医療機器ソフトウェアシステム検証サービス
IEC62304等の医療機器ソフトウエア規格を考慮した、
テストプロセス構築からテストオペレーション全般を支援
- こんな方にお勧めします
-
- 医療機器開発事業者様
- 医療分野に新規参入もしくは海外への商品展開をはかりたいお客様
- こんな悩みを解決します
-
- 内製体制では、第三者性がないため、仕様の抜け漏れがあり、品質が上がらない
- 限りある自社の技術者は、設計・開発業務に集中させ、開発効率を向上したい
- 規格要求事項に適合した検証を実施したいが、そのために必要なタスクが把握できていない
- 開発期間が短いことから、必要な文書を作成する時間がない
医療機器ソフトウェアシステム検証サービスとは
平成26年 (2014年) 11月25日施行の医薬品医療機器等法において、医療用単体プログラムも医療機器とされ、承認・認証が必要になりました。そのため、ソフトウェアの開発においては、諸外国向けの申請時と同様に、医療機器ソフトウェアのライフサイクルプロセスに関する国際規格である、IEC 62304への準拠が必須となります。
本サービスは、IEC 62304等の医療規格を考慮したテストプロセスの構築を支援し、第三者の視点でテストを実行し、テスト工程全般の記録文書を提供するものです。
特 色
医療規格を考慮したシステムテスト業務を、ご予算に応じた最適な計画でアウトソース可能
POINT 1
各種医療規格に準拠したテスト
FDA、IEC62304、ISO13485、ISO14971など、各種規制、規格で要求されるプロセス、アクティビティ、タスクに沿ったテスト業務を実施します。
POINT 2
開発プロセス全体へのアプローチ
担当するのはテストフェーズですが、要求される開発プロセス全体の規格適合に向けて、上流工程の設計担当者に対して、トレーサビリティ確保のための提案や、規格に準拠したテンプレートの提案なども実施可能です。
サービス構成
医療機器ソフトウェアの開発プロセスで特に重要な、「リスクマネジメント」や「トレーサビリティの確保」もご支援します。
| アクティ ビティ | タスク | 概要 | 成果物 | 関連する 規格要件 |
|---|---|---|---|---|
| テスト計画 | システム テスト計画 | 開発計画書、ソフトウェア要求仕様書をレビューし、開発計画に基づくシステムテスト計画書を作成する | ソフトウェア 検証計画書 | IEC62304、FDA、ISO13485 |
| テスト設計 | テスト要求分析 | ソフトウェア要求仕様書をレビューし、検証する観点を抽出し、テスト観点マトリクスを作成する | テスト観点 マトリクス | FDA、IEEE829 |
| テスト設計 | テスト観点マトリクスを基にしたテストのアーキテクチャ設計を行い、テスト計画書を作成する | テスト設計書 | FDA、IEC62304、IEEE829 | |
| リスク分析 | リスクマネジメント支援 | ソフトウェアハザード分析書をレビューし、ハザードの軽減対策を第三者観点でチェックする | リスク分析書 | ISO14971、IEC62304、FDA |
| リスクベース テスト計画 | リスク診断結果を基にリスクベーステストを作成しリスクベーステストを計画する | リスクベース テスト計画書 | ISO14971、IEC62304、FDA | |
| テスト実装 | テスト実装 | テスト仕様書(手順書等)を作成する | テスト仕様書 | FDA、IEC62304、IEEE829 |
| トレーサビリティ | 要求、仕様とテスト項目とのトレーサビリティを管理する | トレーサビリティ マトリクス | FDA、IEC62304、ISO14971、ISO13485 | |
| テスト管理 | テスト実行/管理 | テスト仕様書(手順書)を実行する | テスト結果 | |
| 日々のテスト進捗を管理/報告する | 進捗グラフ等 | |||
| 日々のテストで検出した不具合を管理/報告する | インシデント 報告書 | |||
| 完了報告 | テスト結果 記録作成 | 各テスト結果、トレーサビリティ結果、リスクベースド結果をまとめ、報告する | テスト概要 報告等 | FDA、IEC62304、ISO14971、ISO13485 |
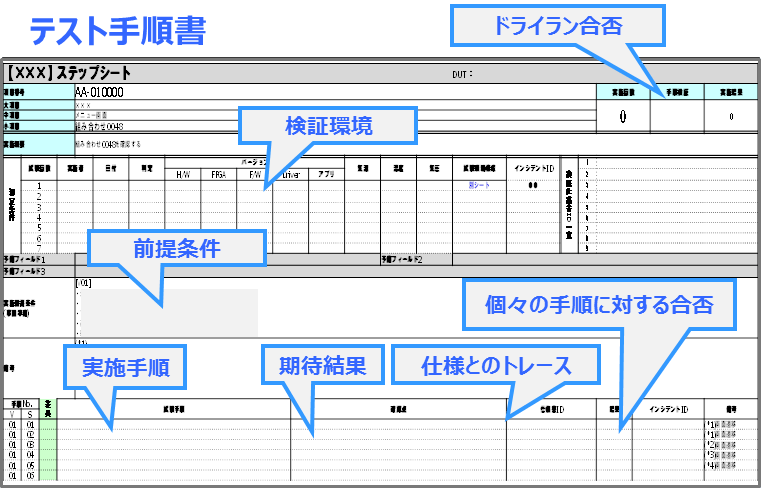
成果物サンプル
あくまで一例です。対応する規格や安全クラス分類などを考慮し、最適で実践的なテーラリングを施します。
お電話でのお問い合わせ(受付時間:平日9:00-17:45)
Webからのお問い合わせ